摘要
目的: 前列腺癌的局灶性不可逆电穿孔 (IRE)纳米刀治疗 旨在减少生活质量并发症,但结果数据仍然有限。本文旨在评估 IRE术 后 ≥12 个月前列腺癌的组织学现场清除率。
材料和方法: 回顾性回顾 2018 年 8 月至 2021 年 8 月期间接受治疗的系列患者的前瞻性获取数据,明确复发的定义为 ≥6 mm 核心 Gleason 3+3 或 ≥Gleason 3+4,肿瘤长度为 ≥4 mm。还分析了国际泌尿病理学会 (International Society of Urological Pathology, ISUP)定义的局部 ≥2 的数据。
结果: 整个系列的中位随访时间为 23 个月(范围 3-39 个月)。在 64 例主要 IRE 手术中,40/50 (80.0%) 进行了监测检查,随访时间为 ≥12 个月。3/40 (7.5%)或 4/40 (10.0%) 发生明确的场内复发, 局部ISUP >2;明确的场外复发发生在 5/40 (12.5%)。挽救性IRE组3例(3/6,50.0%)前列腺特异性抗原水平检测不到,2例活检无残留癌,1例患者视野外复发。对于性活跃的男性,首选纳米刀治疗(IRE)24/28 (85.7%) 维持勃起功能,未发生尿失禁 (0/64)。
结论:前列腺癌局部首选(IRE)纳米刀治疗,90% lSUP >2 的病灶能场内消融,尿失禁或阳痿的风险较低。尽管 IRE 后多参数磁共振成像 (mpMRI) 正常,但仍需要监测前列腺活检以排除进展。挽救性 IRE 是前列腺放疗后局部复发的一种有前景的选择,发病率低。
关键词:局部治疗;不可逆电穿孔;前列腺癌;监测活检;尿失禁
前言
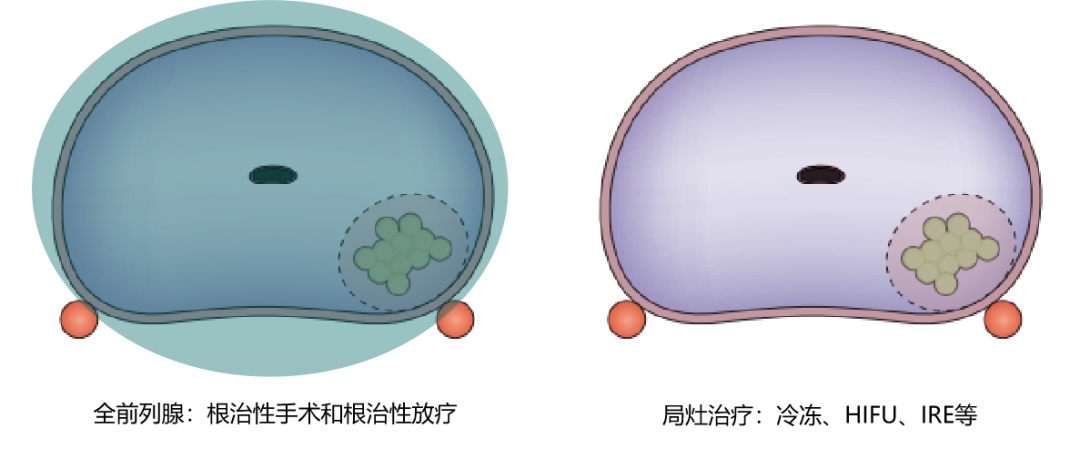
前列腺癌 (PCa) 传统上通过整体疗法和根治性前列腺切除术或放射治疗(包括近距离放射治疗)进行治疗。PCa 的整体治疗与潜在的生活质量副作用有关,包括但不限于尿功能不全、阳痿和对肠道/膀胱的辐射毒性。
局部治疗前列腺癌,旨在最大限度地减少生活质量并发症,同时降低其进展的风险。最初主要集中在低风险和中度风险前列腺癌的处理,因为这类病人即使采用观察处理,诊断后10年内的特异性死亡率也较低[1-3]
有许多不同的局部治疗技术,包括高强度聚焦超声消融、局部冷冻疗法、局部近距离放射治疗和局部激光消融。然而,目前尚无前瞻性的局部治疗技术间的前瞻性直接比较试验,也没有现有数据支持任何技术更优越[4,5]。不可逆电穿孔(Irreversible electro-porusion, IRE)是一种局部疗法,它利用针电极之间的脉冲电流引起组织消融,产生非热凋亡而不是凝固性坏死[6,7]。IRE改变细胞膜,不可逆地增加细胞的通透性,导致渗透不平衡和凋亡。重要的是,使用IRE技术,血管和平滑肌细胞等结构似乎更能抵抗损伤[8]。早期临床数据显示,前列腺癌的现场清除率良好,副作用毒性最小,包括尿失禁风险低[9-12]。此外,IRE并发症并不常见,通常为Clavien-Dindo分类1-2级[4,13]。
本研究的目的是评估前列腺癌局灶性 IRE 的肿瘤学表现,首先是治疗后大于12个月的活检,了解癌症的组织学现场清除;其次还包括术后并发症、尿失禁和勃起功能障碍的回顾。
材料和方法
对 2018 年 8 月至 2021 年 8 月期间接受 IRE 治疗的系列患者的单一机构多外科医生队列的前瞻性获取数据进行了回顾性评价。获得 Uniting Care Health 人类研究伦理委员会的伦理批准(批准号:2021.21.359。基于前列腺特异性膜抗原正电子发射断层扫描/计算机断层扫描(PSMAPET/CT)的局限性 PCa 患者被纳入IRE治疗。所有患者都需要进行术前多参数磁共振成像 (mpMRI),具有前列腺外扩展或精囊浸润(T3a/T3b 期)的放射学证据的,都被排除在 IRE治疗外。mpMRI 上最大直径为 ≥25 毫米的肿瘤被认为不适合 IRE ,仅根据前列腺特异性抗原 (PSA) 水平或前列腺内的任何特定解剖肿瘤位置,患者不会被排除在外。IRE 治疗区基于经阴前列腺活检阴性或阳性结果,结合mpMRI 前列腺成像报告和数据系统 (PIRADS)3-5 病灶,或者治疗前分期 Ga-PSMA PET/CTcan一致性。在 IRE 程序之前,所有患者都得符合明确前列腺癌的标准,该标准基于“≥6 毫米核心国际泌尿病理学会 (ISUP) 1 级 (Gleason 3+3) 或 ISUP 2 级 (Gleason 3+4) 肿瘤长度为 ≥4 毫米,或 ISUP 3-5 级的任何病灶”。
都是由外科医生自行决定的首次双侧肿瘤 IRE治疗,仅在先前放疗后的挽救性治疗中进行单侧消融。纳米刀治疗前都进行前列腺活检,以排除 IRE 治疗区以外的明确体积或格里森分级的病灶。如果患者之前在另一个中心接受过 IRE,他们也会被排除在外。
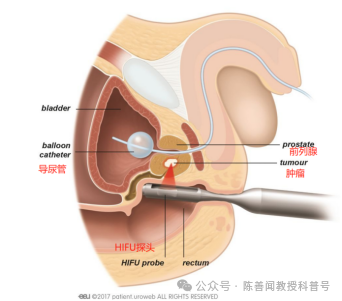
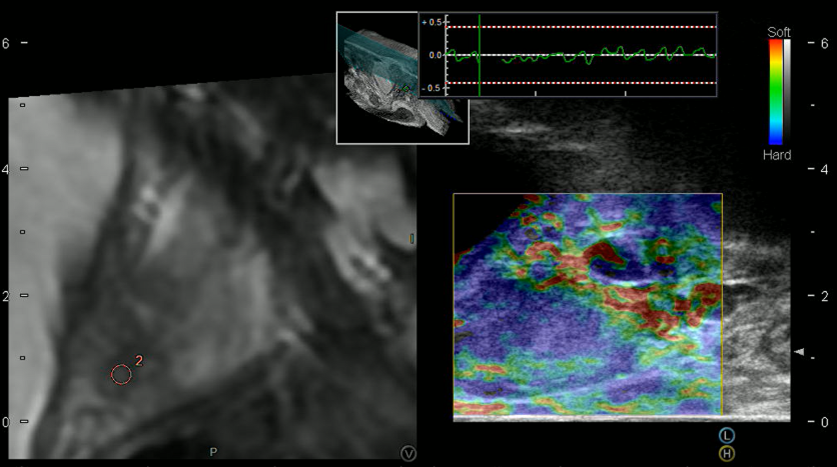
IRE 手术是在全身麻醉下进行的,患者处于截石位置,导尿管原位放置。治疗野大小是基于经会阴 IRE 针在 MRI 病灶周围的合适放置,最小边缘为 5 mm(图 1)。通过经直肠超声探头图像,在轴向和矢状切片中确认 IRE 针的位置。插入的 IRE 电极针的数量取决于病变的大小和形状。IRE 针头位于距重要结构(直肠壁/尿道)≥4 毫米处,极性变为正极,以避免任何潜在的热损伤。最初常使用术前磁共振影像与术中经直肠超声 (MRI-TRUS)图像融合的方法,帮助精确放置针头,但由于泌尿外科医生在经会阴活检和近距离放射治疗技术方面的经验丰富,针放置已无需(MRI-TRUS)图像融合。然后将 IRE 针连接到 NanoKnife(Angiodynamics PTL,Latham,NY,USA),基于机器的计算机治疗计划软件,该机器控制电流。最初应用一组 10 个脉冲来确定组织的电导率,然后是 80 个脉冲的治疗序列。调整了机器参数,目的是尽可能在探头对之间实现电流变化最小>9安培 (Amps)。一般来说,我们的目标是 IRE 针之间的距离为 15 毫米(10-22 毫米),电流为 25 安培(20-35 安培),电压为 2,500 伏(1,500-3,000 伏),针头暴露长度为 15 至 20 毫米。

留置导管拔除的时间取决于个体外科医生的偏好,尽管在我们机构中,患者最初会在原位留置导管 (IDC) 下过夜以进行观察。术后并发症评定是基于 Clavien-Dindo Clas- sification 系统。尿失禁被定义为术后期间对尿垫的任何要求。勃起功能被定义为根据国际勃起功能指数 (IIEF-5) 评分的问题 1 获得和保持勃起的中等(或更高)信心,或根据扩展前列腺癌指数综合 (EPIC) 问题获得勃起的小问题或没有问题。如果患者未完成治疗前后的 EPIC 问卷或 IEF-5 表格,则通过独立于外科医生的研究者联系患者,以确认失禁和勃起功能。
主治泌尿科医生建议所有患者在 IRE 后 6 个月进行 mpMRI 检查,并在术后至少 12 个月对内场治疗区和场外前列腺组织进行常规监测模板经会阴活检。组织病理学在泌尿病理科的专门部门进行了审查。mpMRI 图像由一家机构报告,该机构每月进行 >200 次前列腺 mpMRI 手术。只有进行了至少 10 次 IRE 手术的外科医生才被纳入分析。
监测前列腺活检的显着肿瘤复发定义为 ≥6 mm 核心 ISUP 1 级 (Gleason3+3) 或 ISUP 2 级 (Gleason 3+4),肿瘤长度为 ≥4 mm,或任何 ISUP ≥3 级病灶。正核心长度为<4 mm的病变与整个组织病理学检查的肿瘤体积<02 mL有关[14]。任何尺寸的病灶格里森评分 3+4(ISUP 2 级),作为明确癌症病灶的第二个定义。
结果
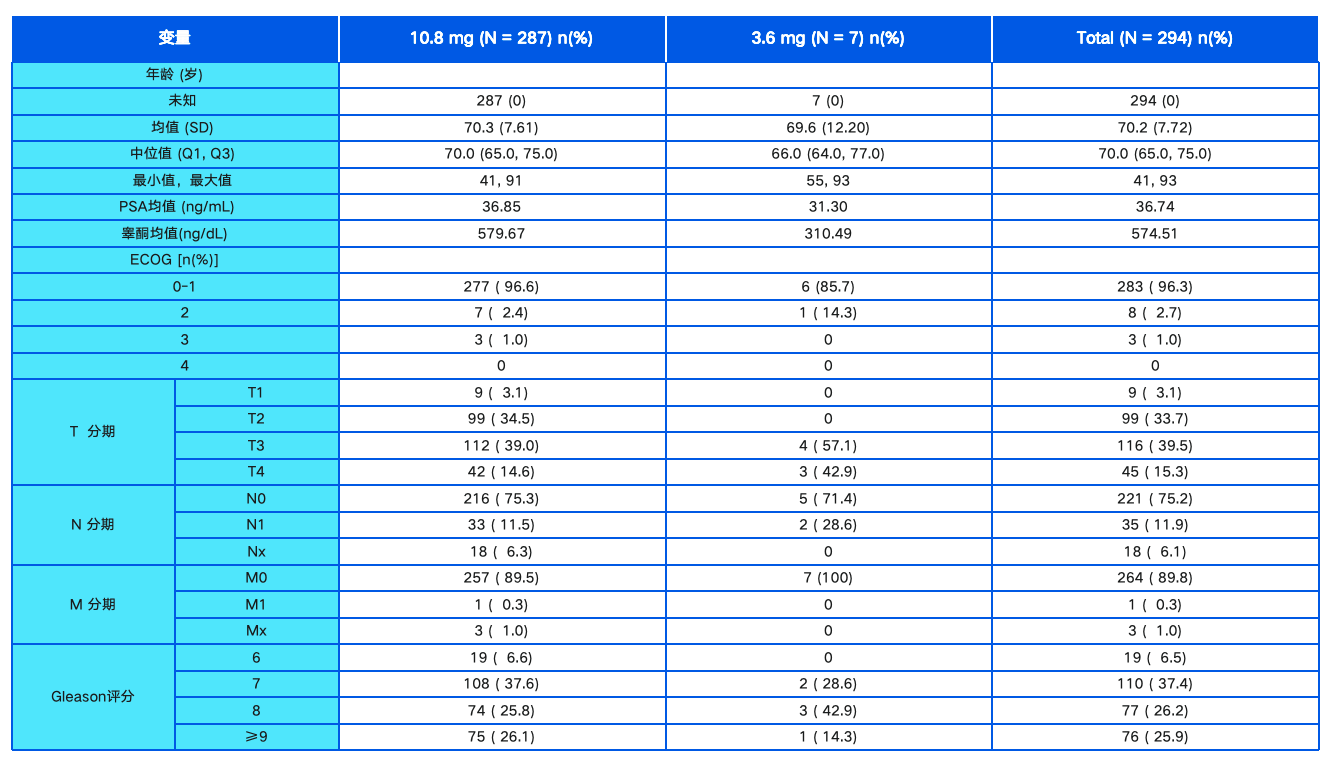
2018 年 8 月至 2021 年 8 月期间,有 70 名男性接受了局灶性 IRE 治疗。所有患者在 IRE 治疗区都有显着的症状。64/70 例患者进行了首选 IRE,其中 4 例双侧病灶消融。对 6 例患者进行放疗后挽救 IRE 以防局部复发。表 1 和表 2 概述了诊断时系列的特征。中位随访时间为 23 个月(范围 3-39 个月)。中位年龄为72岁(范围51-87岁)。在研究的70例患者中,64例在IRE当天或术后第一天出院(64/70,91.43%)。最多停留时间为两天。没有患者在 30 天内因治疗后并发症而需要再次入院。


1. 首选IRE治疗
在接受首选IRE 治疗的 64 名男性中,有 50 名随访超过 12 个月(中位数 23 个月,范围 3-39 个月)。中位数 PSA 为 6.10 ug/L(范围 0.77-25.00 ug/L)。中位 ISUP 分级为 2 级,其中 12 例患者接受高危 ISUP 4-5 级恶性肿瘤治疗。大多数患者在诊断时进行了 PI-RADS 4 mpMRI(44/64),只有 4 例患者进行了低风险 PI-RADS 2 mpMRI。42/64 例患者无对侧肿瘤,17/64 例为野外 ISUP 1 级,4/64 例为 ISUP 2 级,1 例患者对侧叶 ISUP 3 级病灶为 l mm 病灶。在随访≥12个月的男性中,治疗前PSA密度的中位数为0.13(范围0.02-0.55)。该系列的中位 PSA 最低点为 13 ug/L(范围 0.07-7.20 ug/L)。PSA最低点为IRE前PSA原水平的1.10%至114.55%,中位数为26.5%。
1) 首选IRE 的随访活检数据
40/50 (80.0%) 的患者通常在初次 IRE 后随访 12 个月进行监测活检,但在 IRE 第 2 年进行 4 次活检,在 IRE 后 3 年进行 3 次活检。其余患者要么因 PSA 水平低而拒绝活检和/或在 IRE mpMRI (PI-RADS ≤2) 后完全消融。在 35/40 (87.5%) 的监测活检中发现所有现场癌症完全消融。3/40 (7.5%) 的监测活检发现显著的现场复发,使用任何 ISUP 2 或更高级别的定义 2 发现 4/40 (10.0%)(表 3、4)。一名患者病灶小,病灶不显着的现场 ISUP 1 级恶性肿瘤。此后,两名明显野内复发的患者进行了机器人辅助腹腔镜根治性前列腺切除术 (RALP),分别展示了 Gleason 3+4 和 4+3。两者患者的RALP组织病理学检查结果为pT2,边缘为阴性。第三位患者正在等待RALP检查,第四位患者由于ISUP 2级恶性肿瘤的微小部分而选择保守治疗。在4例局部复发且ISUP≥2的患者中,术前PSA密度为0.12(0.08-0.14),PSA最低值中位数为3.2微克/升(1.4-4.2微克/分升),与初始PSA相比,PSA最低值的中位数为58.00%(23.73%-91.43%),5/40(12.5%)的监测经会阴穿刺活检患者和11/40(275%)的任何ISUP 2级病灶(定义2)患者中,有显著的病灶外复发。诊断时无对侧肿瘤,25/42 在 IRE 后进行了活检。5/25 的监测活检发现场外 ISUP 2 级癌症,但只有 1 名患者的肿瘤核心长度为 >4 mm。在诊断时对侧叶 ISUP 1 级的 17 例患者中,l1 例进行了监测活检,其中 4 例进展为 ISUP 2 级,2 例患者的核心长度为 ≥4 mm。4 名对侧 ISUP 2 患者中有 3 名在监测活检时有类似的恶性肿瘤,另一名有明显的系统核心。病灶为野外 ISUP 3 级的患者尚未进行监测活检。在接受双侧 IRE 病变治疗的 4 例患者中,1 例进行了场内复发挽救性 RALP,2 例在两种定义下均有显着的场外复发,只有 1 例 IRE 活检后阴性。
2) MRI 主要队列数据
基线 mpMRI 结果如表 1 所示。PI-RADS 4 是 preIRE mpMRL 中最常见的病变 (44/64, 68.8%) 对 52/59 名初次后 6 个月以上的男性进行了 IRE 后 mpMRI。愤怒。mpMRI 通常在 IRE 后 6 个月进行,但 3 名患者在 IRE 后 10 至 18 个月进行 mpMRI,3 名患者在前 3 个月内进行了 mpMRI。低风险 PI-RADS 2 发现在 46/52 (88.46%) 中明确,其中 PIRADS 3/3,PIRADS4 1 例,PIRADS 5 例。在 IRE PI RADS 2 后队列中,33/46 有监测活检数据,根据两种显着性定义,2/46 队列中发现了重要的现场癌症。在模板活检中,3/33 (9.09%) 或 8/33 (24.24%) 发现任何体积 ISUP 2 级的显着场外癌症。对于显著的 PCa,ISUP 2 级恶性肿瘤病灶的阴性预测值为 73.7% (28/38)。6 名 PI-RADS 3-5 mpMRI 异常男性中有 5 名在 IRE 后 12 个月进行监测活检。所有患者均患有癌症,但在 3 名患者中,使用这两种定义都确定了严重的癌症,mpMRI 的阳性预测值为 60%。
3)高危人群的结果(ISUP分级4&5)
有 12 名高危 PCa 患者(ISUP 4 和 ISUP 5 各 6 名)接受了首选 IRE。IRE 后 mpMRI 呈低风险 PI-RADS 2 的有 10 名患者,2 名患者拒绝继续随访 mpMRI。该队列中有 7 名患者接受了活检(1 名在 IRE 后 2 年,1 名在 IRE 术后 3 年),3 名患者由于随访时间 <12 个月而无需活检,1 名患者因 PSA 水平低而拒绝活检,1 名因发生与 IRE 无关的 Wernicke 脑病而拒绝活检。高危组无局部复发(0/7,0%),但 1 名患者出现明显的远处复发,7 名患者中有 3 名(42.86%)出现明显的远处复发。
4)原发性IRE的并发症
所有 64 名接受原发性 IRE 治疗的男性均保持无尿失禁,尿失禁率为 0%。一名患者在重复对侧 IRE 手术后出现尿失禁。在 50 名接受随访 ≥12 个月的男性中,有 28 名在术前具有正常的勃起功能,其中 24 名(85.71%)在首选IRE 治疗后保持正常勃起功能。只有一名患者出现 Clavien-Dindo ≥ 2 级并发症,该患者在术后 3 个月时要求扩张尿道狭窄,与左侧中前角周边区肿瘤的 IRE 手术无关。
2. 挽救放射治疗失败的IRE
6例挽救性放疗失败。挽救性放疗的中位随访时间为22个月(范围为13-30个月)。挽救性放疗的基线PSA中位值为2.20微克/升(范围为1.3-3.0微克/升)。0.24-8.4微克/升)。放射治疗后,术前活检结果显示,5名患者的IS UP分级<4,1名患者的IS UP分级为5。在挽救性IRE之前,有4名患者没有局部肿瘤,1名患者对侧叶有小的IS UP 2级病灶,另一名患者有小的IS UP 5级病灶。
3. 在挽救性切除术后,3名患者(3/6,50.0%)的PSA水平检测不到,所有患者PSA均<0.55ug/L(范围 0-0.53 ug/L)。
1) 挽救 IRE治疗,随访 mpMRI 和活检数据
3 例患者在挽救 IRE 后进行了监测 mpMRI 扫描,均为低风险 PI-RADS 2。其他三名患者由于 PSA 水平低/无法检测到而拒绝 mpMRI 随访。2 例患者在挽救 IRE 后进行了经会阴监测活检,均为良性反应,无残留的场内或场外 PCa。一名患者在 IRE 后 7 个月进行的 TURP 芯片中,Gleason 评分为 3+4,该芯片用于治疗膀胱流出道梗阻 7 个月。其他三名患者由于无法检测到PSA水平而拒绝监测活检。1 例患者在挽救 IRE 前进行活检显示为 5 级高危 ISUP。他的 IRE 后 mpMRI 为 PIRADS 2,患者拒绝活检,因为 IRE 后的 PSA 为 <0.008 ug/L。2)放疗失败挽救性IRE的并发症 没有Clavien-Dindo >2级并发症。在 2/6 的挽救性 IRE 手术中因 ra-diotherapy 失败而发生尿失禁,尽管尿失禁仅在两名患者随后接受 TURP 治疗 blad 后发生。DER 流出阻塞。6 名患者中只有 2 名患者在挽救 IRE 前有效,1 名 (50%) 在 IRE 后保持勃起功能。
讨论
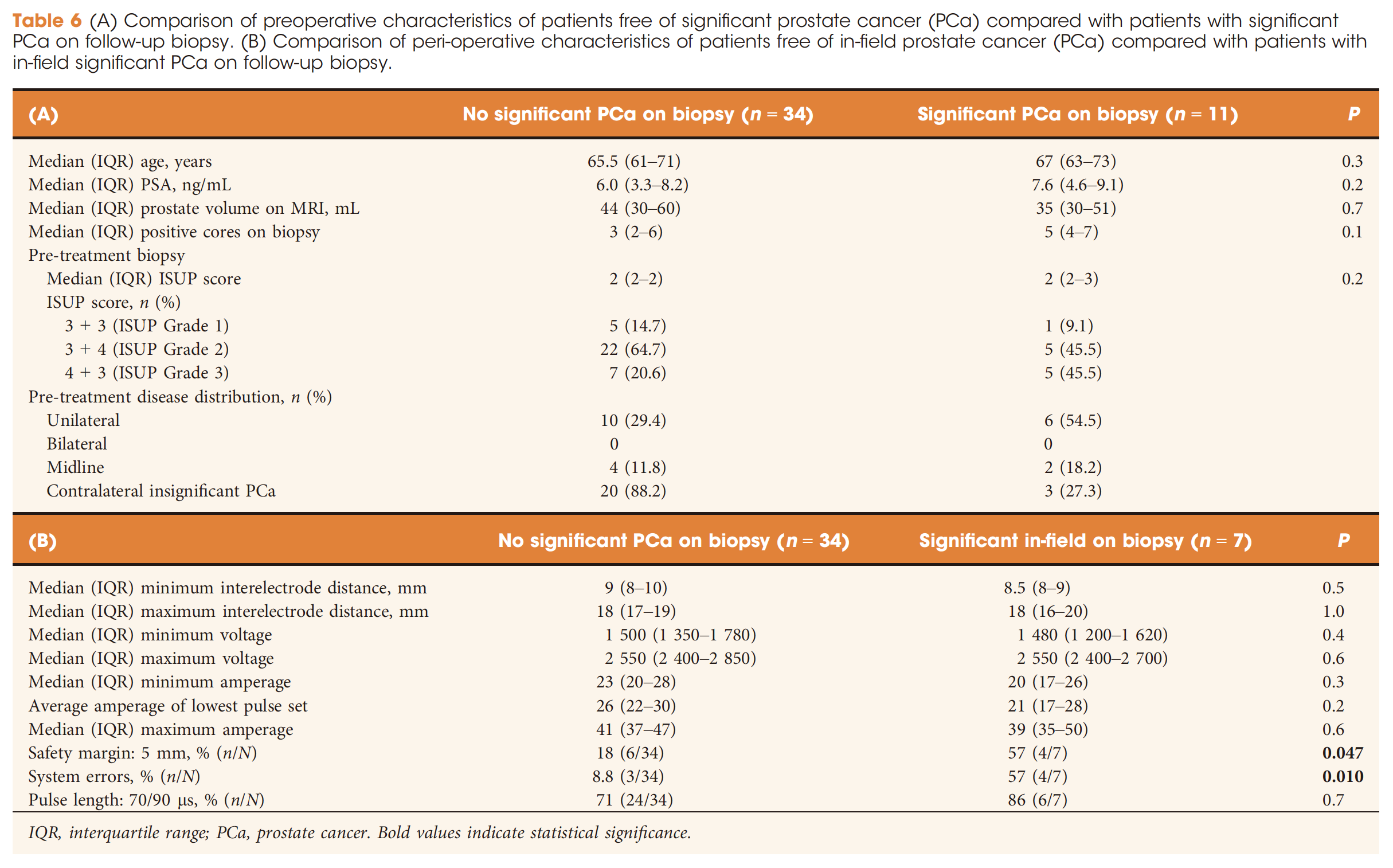
局部治疗的目的是获得肿瘤的肿瘤学清除,同时避免重大的治疗并发症并保持生活质量。在关于局灶性IRE的系统评价[4,13]中,只有两个系列研究的患者数量比我们的研究多,其中最大的研究是异质性系列,没有区分局灶性IRE与半消融术或全腺IRE的结局[11]。因此,本手稿增加了有关局灶性 IRE 结果的重要信息。在我们的主要 IRE 系列研究中,所有癌症的组织学现场清除率是 87.5%。 场内复发率为 7.5%;如果包括 ISUP 2 的任何小核心长度,则为 10.0% ,模板监测核心活检的场外癌症复发率为 5/40 (12.5%)。当将 ISUP 2 级的任何核心长度视为复发时,场外复发率从 IRE 前的 5/40 (12.5%) 增加到监测活检时的 11/40 (27.5%)。场外肿瘤进展不是局灶性 IRE 技术的失败,而是患者选择的失败。如果在 IRE 之前进行模板活检的没有场外病灶,5/25 发展ISUP 2 级场外进展,在监测活检中,但只有 1 名患者 (4.0%) 的癌症核心长度为 ≥4 mm。我们的结果表明,作为 IRE 后主动监测方案的一部分,持续的前列腺活检监测是必不可少的,因为尽管在 IRE 后早期随访中 mpMRI 风险较低,但仍可能发生严重的 前列腺癌。
我们的研究结果证实了令人满意的已发表的原发性前列腺癌在 IRE 后的早期功能结果。在我们的研究中,在首选IRE 环境中没有出现尿失禁。然而,一名最初在 IRE 后处于大陆状态的患者在第二次 IRE 消融术后因对侧叶的新病变而出现失禁。这与其他已发表的系列研究一致,即治疗后12个月患者的尿功能正常占88%-100%[13]。然而,在初次前列腺放疗后挽救局部复发的 IRE 后,尿失禁风险增加。6 名男性接受了 IRE 治疗外照射放疗后的局部复发。最初没有 IRE 后尿失禁,但其中两名患者随后进行了 TURP 治疗膀胱流出道梗阻,并且两人都在 TUR 尿失禁后发展,每天需要一个失禁垫。
在随访超过12个月的男性中,28/50在首选IRE前有性功能,24/28(85.7%)保持适合的主要性功能,有或没有PDE抑制剂。在其他已发表的系列研究中,勃起功能维持在50%-100%之间,其中在挽救环境中使用EPIC问卷评估时,勃起功能保留的效力率为77%[15]。我们系列中的 6 名患者中只有 2 名在挽救 IRE 前有性功能,其中 1 名患者 (50%) 在挽救 IRE 后保持了令人满意的勃起功能。
国际Delphi共识建议,局部治疗后的肿瘤学结局应包括血清PSA、mpMRI和系统/靶向前列腺活检结果[16]。我们认为,使用IRE后PSA作为成功的标志仍然是有争议和不可靠的,因为不同前列腺体积的PSA水平、IRE消融的组织量和前列腺炎症的差异。在Blazevski等[12]对123例中度(91%)或低危癌症男性的研究中,PSA中位数从5.725ng/mL下降到3.48ng/mL(四分位距143-5.67)IRE后,在50例接受IRE治疗的心尖瘤患者中,PSA下降了71%[17]。这几乎与我们初始 PSA 水平的 26.5% 的 PSA 最低点中位数相同。在我们的研究中,四名男性的 PSA 下降百分比较低,主要治疗是现场复发,但较小的数字妨碍了统计分析。mpMRI 已被用作替代标志物来识别局部治疗(包括 IRE)后的复发,但 IRE 后 mpMRI 在确定局部复发方面的准确性的循证评估并不可靠。在Scheltema等[18]系列研究中,10/33男性在IRE后6个月mpMRI阴性,在IRE前列腺活检组织学检查中检测到癌症,由于持续性癌症的概率低,因此野内复发的阴性预测值高达88%。在我们的系列中,mpMRI 在监测活检中排除任何场内或场外 ISUP 2 级的阴性预测值仅为 73.7%,因此临床医生不应单独依赖 mpMRI 进行局部治疗后的长期监测。
Collettini等[2]先前曾评估过组织学活检结果,他们分析了IRE前列腺后6个月的28例患者。28 名男性中有 2 名 (7.1%) 有临床意义的现场复发。令人感兴趣的是Ting等[10]的分析,他们分析了25名MRI上可见Glea-son评分为<8且PI-RADS为3-5的男性。在 IRE 后 7 个月的前列腺活检中,没有内场复发 (0%),然而,4/21 (19%) 的癌症复发发生在治疗区附近。这一结果与Franklin等[19]在PCa诊断环境中的活检结果相似,当靶区呈阳性时,他们在77%的病例中发现了近靶区有显著的癌症,其中17%的受试者通过增加近靶区核心进行了升级。这些发现概述了最小IRE边缘治疗区5 mm的重要性,因为与放射状前列腺切除术组织学相比,mpMRI可能低估组织学肿瘤体积[20]。国际Delphi共识仅推荐对D'Amico低/中危癌症进行局部治疗,包括ISUP 3级[21]。与此相反,我们在首选 IRE 后的监测活检中发现了所有高危 ISUP 4-5 级恶性肿瘤的现场消融术。该队列的长期结果将受到密切监测。
IRE 成功的定义应通过癌症的内场组织学清除率来评估。IRE 活检后数据仍然是评估肿瘤消融的金标准。尽管专家(小组)对局部治疗后随访活检的共识提出了建议,但并非所有患者都愿意遵守这些建议[22,23]。局部治疗试验后IRE活检的国际比率从17%到100%不等[4]。在我们的系列研究中,76% 的男性在随访 12 个月后同意进行监测前列腺活检。由于 PSA 水平低与低风险 PI-RADS 2 mpMRI 发现相关,其余研究被排除在首位。在原发性 IRE 之后,在我们的系列中,35/40 (87.50%) 没有任何场内恶性肿瘤。这证实了令人鼓舞的早期数据表明,IRE是治疗领域内PCa控制的可靠技术。在监测系统活检中,显著的场外癌症的升级并不一定是局部治疗失败,而是选择过程失败,或者在初始评估时未能识别出显著的体积恶性肿瘤。鉴于局部治疗缺乏长期总体生存期和无转移生存期,因此必须将未诊断的风险降至最低。在局部治疗之前鼻中有明显的场外肿瘤。
关于放射性复发性 PCa 挽救性 IRE 结果的数据很少。Scheltema等[15]分析了18例患有局限性放射性复发PCa的男性,其中3名男性存在基于Phoenix定义的生化衰竭。然而,Phoenix的定义严重低估了放疗后癌症复发的可能性,一旦放疗后PSA水平升高到0.5以上,PSMA PET/CT就会越来越多地发现这一点[24]在我们的队列中,6名接受挽救性IRE治疗局部复发的患者中,PSA<为0.01ng/L,中位随访时间为22个月(范围13-30个月),其他3名患者的PSA均为1/0.01ng/L,其他3名患者的PSA均为1<0.55 ug/L 与其他治疗(如挽救性根治性前列腺切除术)相比,挽救性 IRE 手术耐受性良好,副作用最小,没有初始尿失禁。然而,根据我们的结果,鉴于尿失禁的风险增加,在放疗后队列中挽救 IRE 后进行 TURP 时建议谨慎。
我们研究的局限性包括相对较短的随访和对前瞻性 da-tabase 的回顾性审查。在回顾性研究中,并发症可能被低估;然而,除了两名患者在IRE后重新安置在海外并在最后一次随访中被审查外,我们对所有患者都进行了完整的随访。
结论
根据 IRE纳米刀 术后活检,原发性前列腺癌的局部 IRE纳米刀治疗,癌症的完全现场清除率 87.5%,或 ISUP 2 级任何核心长度的清除率是 90%。术后并发症极少,治疗后尿失禁或阳痿的风险低。即使 IRE 后 mpMRI 检查正常,但仍需要前列腺活检监测,以排除治疗区内或治疗区外的进展,IRE 是前列腺放疗后局部复发的一种有前途的补救性选择,致残率低。